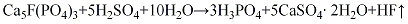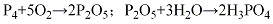化学性质
中文名 磷酸
外文名 Phosphoric acid
别名 正磷酸
化学式 H₃PO₄
分子量 98

CAS登录号 7664-38-2
EINECS登录号 231-633-2
物性数据
1.性状:纯磷酸为无色结晶,无臭,具有酸味。
2.熔点(℃):42.4(纯品)
3.沸点(℃):260[3]
4.相对密度(水=1):1.87(纯品)
5.相对蒸气密度(空气=1):3.38
6.饱和蒸气压(kPa):0.0038(20℃)
7.临界压力(MPa):5.07
8.辛醇/水分配系数:-0.77
9.溶解性:与水混溶,可混溶于乙醇等许过有机溶剂。
毒理学数据
1.急性毒性 LD50:1530mg/kg(大鼠经口);2740mg/kg(兔经皮)
2.刺激性
家兔经皮:595mg(24h),重度刺激。
家兔经眼:119mg,重度刺激。
3.亚急性与慢性毒性 动物长期吸入10.6mg/m3,使血清蛋白含量增加及肝糖原降低。
生态学数据
1.生态毒性 TLm:138mg/L(96h)(食蚊鱼)
2.生物降解性 暂无资料
3.非生物降解性 暂无资料
分子结构数据
1、摩尔折射率:13.52
2、摩尔体积(cm3/mol):45.2
3、等张比容(90.2K):154.4
4、表面张力(dyne/cm):136.3
5、极化率(10-24cm3):5.36
计算化学数据
1、疏水参数计算参考值(XlogP):-2.1
2、氢键供体数量:3
3、氢键受体数量:4
4、可旋转化学键数量:0
5、互变异构体数量:无
6、拓扑分子极性表面积(TPSA):77.8
7、重原子数量:5
8、表面电荷:0
9、复杂度:49.8
10、同位素原子数量:0
11、确定原子立构中心数量:0
12、不确定原子立构中心数量:0
13、确定化学键立构中心数量:0
14、不确定化学键立构中心数量:0
15、共价键单元数量:1
性质与稳定性
1.具潮解性。其酸性较硫酸、盐酸和硝酸等强酸为弱,但较醋酸、硼酸等弱酸为强。经高温加热约200℃便失水成焦磷酸,超过300℃为偏磷酸。有腐蚀性。受热分解产生剧毒的氧化磷烟气。接触强腐蚀剂,放出大量热量,并发生溅射。
2.稳定性 稳定
3.禁配物 强碱、活性金属粉末、易燃或可燃物
4.避免接触的条件 受热、潮湿空气
5.聚合危害 不聚合
6.分解产物 氧化磷
贮存方法
储存注意事项 储存于阴凉、通风的库房。远离火种、热源。库温不超过30℃,相对湿度不超过80%。包装密封。应与易燃物、碱类、活性金属粉末分开存放,切忌混储。储区应备有合适的材料收容泄漏物。
安全信息
安全防护
磷酸无强氧化性,无强腐蚀性,属于较为安全的酸,属低毒类,有刺激性。
LD50:1530mg/kg(大鼠经口);2740mg/kg(兔经皮)
刺激性:兔经皮595mg/24小时,严重刺激;兔眼119mg严重刺激。
接触时注意防止入眼,防止接触皮肤,防止入口即可。
遇H发孔剂可燃; 受热排放有毒磷氧化物烟雾。
磷酸蒸气能引起鼻黏膜萎缩;对皮肤有相当强的腐蚀作用,可引起皮肤炎症性疾患;能造成全身中毒现象。
若有磷酸蒸气入眼,应立即用大量生理盐水冲洗,随后送医院救治。
空气中最高容许浓度为1mg/m3。生产人员工作时应穿戴防护用具,如工作服、橡皮手套、橡皮或塑料围裙、长筒胶靴。注意保护呼吸器官和皮肤,如不慎溅到皮肤,应立即用大量清水冲洗,把磷酸洗净后,一般可用红汞溶液或龙胆紫溶液涂抹患处,严重时应立即送医院诊治。
合成方法
1.工业生产方法有湿法和热法。前者制得磷酸浓度较低,而且含杂质较多,需要进行净化。如以酮-醇混合物为萃取体系精制湿法磷酸,经萃取-洗涤-反萃取和钡盐沉淀净化的工艺流程,已生产出合格的85%工业磷酸。后者制得磷酸浓度和纯度都高,但耗电量大、投资和成本较高。
湿法是用酸分解磷矿石制得。此法分为硫酸法、盐酸法、硝酸法和硫酸氢铵法。常用为硫酸法。硫酸法由于反应温度和制得磷酸浓度不同,在磷酸水溶液中硫酸钙晶体有三种不同形式,按其生产工艺分为“二水物”流程、“半水物”流程、“无水物”流程,近年还出现“半水-二水物”流程和“二水-半水物”流程等。
2.湿法(硫酸法)二水物流程将磷矿石粉碎至80~100目后,加入萃取槽,再加人淡磷酸和返酸以维持料浆的液固比为(2.5~3.5):1(重量比),并调节磷酸浓度。把硫酸按理论量的102%~104%加入萃取槽,与磷矿粉于75~85℃进行萃取反应4~8h。反应后的料浆经过滤,滤液即为磷酸,浓度一般在20%~25%P2O5,其中一部分返回萃取槽调节液固比,另一部分送去蒸发浓缩,制得磷酸成品。其
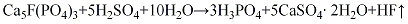
滤渣经多次洗涤后排出,其磷石膏用于制造硫酸的原料,洗液返回萃取槽用。
热法热法磷酸的生产有酸冷流程、水冷流程和喷射除雾流程,现分述如下:
酸冷流程将黄磷在熔磷槽内熔化成液体,经磷喷嘴送人燃烧水合塔,同时用压缩空气(一次空气)将磷雾化,使磷氧化燃烧生成五氧化二磷。为了使磷氧化完全,在塔顶还需补充二次空气。在塔顶沿塔壁淋洒30~40℃的循环磷酸,使五氧化二磷气体冷却,同时与水合成磷酸。排出的气体进入电除雾器以回收磷酸,再经冷却至30~40℃后,大部分作循环磷酸返回燃烧水合塔,小部分作磷酸成品。其
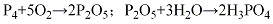
水冷流程将黄磷熔化后,用泵把液态磷送人燃烧室,同时用压缩空气使磷雾化,并补充二次空气,使磷在燃烧室内进行氧化。产生气体温度为800℃左右,在室外用水冷却,使壁温保持80~125℃。从燃烧室出来的气体进入石墨制的气体冷却器,气体经冷却至80℃时进入水合塔,在塔中分三层喷水冷却,并水合成磷酸成品。尾气冷却至100℃以下,经电除雾器排入大气。
喷射除雾流程将液态黄磷经磷喷嘴送入燃烧水合塔,同时用压缩空气使磷雾化,燃烧生成的五氧化二磷立即与水形成磷酸酸雾。将酸雾经热交换器冷却后被喷射除雾器吸人,酸雾在喷射器喉部碰撞,凝集成大颗粒后在旋风分离器内回收,配制成85%H3PO4,制得磷酸成品。
3.制法 以热法还原所生产的工业磷酸为原料,加热至80℃左右,然后通入硫化氢气体达到饱和,密闭静置,使硫化砷和硫化铅沉淀完全,过滤。加热滤液不超过150℃,蒸发,以除去硫化氢和氯化氢气体,浓缩至相对密度等于1.90为止。如需进一步提高质量,可先用上述磷酸用水稀释至相对密度为1.06以下,过滤、蒸发、浓缩至相对密度为1.70(20℃) ,冷却,得到的是松散的含水试剂磷酸。
4.① 黄磷气化后导入空气或过热水蒸气使其氧化,生成五氧化磷,用水吸收,经除砷而得。② 用硝酸使磷氧化而得。③ 磷酸三钙 ( 骨灰)与稀硫酸共热,经分解后,滤出滤液,再浓缩而得。
上下游产品信息
表征图谱
相关文献
用途
农业:磷酸是生产重要的磷肥(过磷酸钙、磷酸二氢钾等)的原料,也是生产饲料营养剂(磷酸二氢钙)的原料。
工业:磷酸是一种重要的化工原料,主要作用如下:
1、处理金属表面,在金属表面生成难溶的磷酸盐薄膜,以保护金属免受腐蚀。
2、和硝酸混合作为化学抛光剂,用以提高金属表面的光洁度。
3、生产洗涤用品、杀虫剂的原料磷酸酯。
4、生产含磷阻燃剂的原料。
食品:磷酸是食品添加剂之一,在食品中作为酸味剂、酵母营养剂,可乐中就含有磷酸。磷酸盐也是重要的食品添加剂,可作为营养增强剂。
医学:磷酸可用于制取含磷药物,例如甘油磷酸钠等。