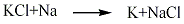金属钾

-
CAS号:
7440-09-7
-
名称:
金属钾
-
英文名称:
——
-
别名:
金属钾
-
分子量:
39.10
-
分子式:
K


 易燃
易燃  腐蚀
腐蚀